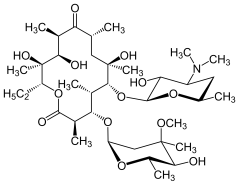
Макроліди
Макролідні антибіотики – це група препаратів з протимікробною активністю, обумовленою наявністю в їх структурі макролідного лактонного кільця.
ІСТОРИЧНА ДОВІДКА
У 1949 р. перший представник макролідного ряду антибіотиків – еритроміцин був виділений зі штаму актиноміцет Saccharopolyspora erythraea, також відомого під назвою Streptomyces erythraeus. Він був створений з метою подолання резистентності пеніциліну в 1953 р. У США еритроміцин вперше надійшов у продаж під назвою «Ілозон».
У 1981 р. група вчених під керівництвом Нобелівського лауреата Роберта Вудворда вперше отримала еритроміцин А шляхом хімічного синтезу. Усі подальші після еритроміцину макролідні антибіотики розроблялися з метою подолання недоліків, властивих еритроміцину. Так, кларитроміцин був синтезований групою японських фармацевтів у 1970 р. для подолання нестабільності еритроміцину в кислотному середовищі шлунка.
МЕХАНІЗМ ДІЇ МАКРОЛІДІВ
Бактеріальні рибосоми складаються з 2 суб’одиниць: маленької 30S і великої 50S. Механізм дії макролідів полягає в інгібіруванні РНК-залежного синтезу білка, шляхом зворотнього зв’язування з 50S рибосомальною суб’одиницею чутливих мікроорганізмів. Блокування синтезу білка приводить до порушення зростання і розмноження бактерій, що свідчить про те, що макроліди є переважно бактеріостатичними антибіотиками. В окремих випадках вони можуть проявляти бактерицидну дію за умов високої бактеріальної чутливості і високої концентрації антибіотика. Окрім антибактеріальної, макроліди мають імуномодулюючу і помірну протизапальну дію.
Азитроміцин відноситься до підгрупи азалідів (у лактонне кільце введений атом азоту) і розглядається як представник IІІ покоління макролідів. У зв’язку з тим, що в останні роки спостерігається антибіотикорезистентність деяких збудників до макролідів, на основі 14-членного лактонного кільця були синтезовані кетоліди – 14-членні макроліди, у яких до лактонного кільця при 3 атомі вуглецю приєднана кетогруппа.
ФАРМАКОКІНЕТИКА
Макроліди відносяться до тканинних антибіотиків, оскільки їх концентрації у сироватці крові значно нижче ніж у тканинах і варіюють у різних препаратів. Найбільш високі сироваткові концентрації макролідів спостерігаються у рокситроміцина, найнижчі – у азитроміцина. При цьому макроліди проникають всередину клітин і створюють високі внутришньоклітинні концентрації. Погано проходять через гематоенцефалічний і гематоофтальмічний бар’єри. Проходять в низькій кількості через плаценту і виділяються з молоком.
Макроліди зв’язуються з білками плазми крові різним ступенем. Найбільше зв’язування з білками плазми відзначається у рокситроміцина (більше 90 %), найменше – у спіраміцина (менше 20 %).
Метаболізуються макроліди в печінці за участю мікросомальної системи цитохрому P-450, метаболіти виводяться переважно з жовчю; ниркова екскреція складає 5-10 %. При цирозі печінки можливе значне збільшення періоду напіввиведення еритроміцину і джозаміцину.
Період напіввиведення препаратів коливається від 1 год (мидекаміцин) до 55 год (азитроміцин). При нирковій недостатності у більшості макролідів (окрім кларитроміцину і рокситроміцину) цей параметр не змінюється.
Параметри фармакокінетики макролідів залежать від класифікаційної приналежності:
- Азитроміцин (15-членний макролід з атомом азоту в структурі молекули) має найбільшу активність проти грамнегативних збудників, кларитроміцин (14членний макролід) – проти Helicobacter pylori, спіраміцин (16-членнйй) – проти токсоплазм і криптоспоридій;
- 14-членні макроліди (особливо еритроміцин) мають стимулюючий ефект на моторику ШКТ, що може приводити до диспепсичних розладів, у 16-членних препаратів цього ефекту не спостерігається.
- 4-членні макроліди руйнуються в печінці з утворенням гепатотоксичних нітрозоалканових форм, тоді як при метаболізмі 16-членних препаратів цих форм не утворюється, що відбивається на відсутності гепатотоксичних ускладнень при прийомі 16-членних макролідів;
- 14-членні макроліди пригнічують активність ферментів цитохрому Р-450 в печінці, що приводить до підвищеного ризику виникнення лікарських взаємодій, 16-членні препарати не впливають на активність цитохрома Р-450 і відрізняються мінімальною кількістю лікарських взаємодій.
- 16-членні макроліди зберігають активність проти ряду штамів стафілококів і стрептококів, резистентних до 14- і 15-членних макролідів.
ПОБІЧНА ДІЯ
Макроліди є однією з найбезпечніших груп антимікробних препаратів. Найчастіше побічна дія макролідров зв’язана із застосуванням еритроміцину. До найбільш характерних побічних реакцій при застосуванні макролідів відносять наступні.
ШКТ: блювота, діарея (частіше за інших їх викликає еритроміцин, що має прокінетичну дію, найрідше – спіраміцин і джозаміцин).
Печінка: транзиторне підвищення активності трансаміназ (холестатичний гепатит), які можуть виявлятися жовтяницею, лихоманкою, пригніченням, слабкістю, блювотою (частіше при застосуванні еритроміцину і кларитроміцину, дуже рідко при використанні спіраміцина і джозаміцина).
Центральна нервова система: порушення координації рухів та слуху (рідко при внутрішньовенному введенні великих доз еритроміцину або кларитроміцину).
Місцеві реакції: флебіт і тромбофлебіт при внутрішньовенному введенні, викликані місцевоподразнюючим ефектом (макроліди не можна вводити в концентрованому вигляді і струйно, вони вводяться тільки шляхом повільної інфузії).
Алергічні реакції (висип, кропив’янка та ін.) зустрічаються дуже рідко.
ВЗАЄМОДІЯ МАКРОЛІДІВ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ
Макроліди, інгібуючи печінкові ферменти монооксигеназної системи, підвищують ризик розвитку небезпечних для життя побічних ефектів непрямих антикоагулянтів, теофіліну, вальпроєвої кислоти, карбамазепіну, препаратів спорин’ї, циклоспоріну, дізопіраміду, бромокріптіну, левоміцетину, циметидину, метилпреднізолону і ін.
Макроліди не рекомендується змішувати в одному шприці з вітамінами групи В, аскорбіновою кислотою, цефалотином, тетрацикліном, левоміцетином, гепарином, діфеніном, оскільки утворюється осад.